Pentan
kemisk forbindelse
Der er ingen kildehenvisninger i denne artikel, hvilket er et problem. (april 2020) (Lær hvordan og hvornår man kan fjerne denne skabelonbesked) |
| Pentan | |
|---|---|
| |
| Generelt | |
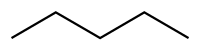
| Systematisk navn | Pentan |
| Andre navne | n-pentan |
| Molekylformel | C5H12 |
| Molmasse | 72,15 |
| Fremtræden | Farveløs væske |
| CAS nummer | [109-66-0] |
| SMILES | ccccc |
| Egenskaber | |
| Massefylde | 0,626 g/cm³ |
| Smeltepunkt | −129,8 °C (143 K) |
| Kogepunkt | 36,1 °C (308 K) |
| Syrestyrkekonstant (pKa) | ~45 |
| Termokemi | |
| Sikkerhed | |
| R-sætninger | R12, R51/53, R65, R66, R67 |
| S-sætninger | S2, S9, S16, S29, S33, S61, S62 |
| Flammepunkt | −49 °C |
| Hvis ikke andet er angivet, er data givet for stoffer i standardtilstanden (ved 25 °C, 100 kPa) | |
Pentan er en organisk kemisk forbindelse, som består af kulstof og brint. Pentan indeholder fem kulstofatomer. Pentan kaldes også n-pentan når alle kulstofatomerne sidder i en lang kæde.
Isomerer redigér
Pentan eksisterer i tre isomere former. Udover n-pentan (CH3CH2CH2CH2CH3) findes også isopentan (2-Methylbutan) (CH3CH(CH3)CH2CH3) og neopentan (2,2-(di)Methylpropan) (CH3C(CH3)2CH3).
| pentan | isopentan | neopentan |
|---|---|---|
Derudover findes en cyclisk forbindelse med 5 kulstofatomer, som kaldes cyclopentan. Dette er dog ikke en rigtig isomer, da den indeholder to brintatomer færre end pentan.
Kemi redigér
Når pentan brænder dannes der kuldioxid og vand.
| Spire Denne artikel om kemi er en spire som bør udbygges. Du er velkommen til at hjælpe Wikipedia ved at udvide den. |