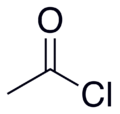
Acetylklorid
Acetylklorid (CH3COCl) er acylkloridet af eddikesyre. Det hører til acylhaliderne, en klasse af organiske forbindelser. Det fremtræder som en farveløs, ætsende, flygtig væske.
| Acetylklorid | |||
|---|---|---|---|
 | |||
 | |||
| IUPAC-navn Acetylklorid | |||
| Generelt | |||
| Systematisk navn | Ethanoylklorid | ||
| Andre navne | Acylklorid | ||
| Molekylformel | CH3COCl | ||
| Molarmasse | 78,49 g/mol | ||
| Fremtræden | Farveløs væske | ||
| CAS-nummer | |||
| SMILES | ClC(=O)C | ||
| InChI | 1/C2H3ClO/c1-2(3)4/h1H3 | ||
| Kemiske egenskaber | |||
| Massefylde | 1,104 g/ml (l) | ||
| Opløselighed i vand | Reagerer med vand | ||
| Smeltepunkt | -112 °C (161 K) | ||
| Kogepunkt | 52 °C (325 K) | ||
| Struktur | |||
| Dipolmoment | 2,45 D | ||
| Sikkerhed | |||
| EU klassifikation | Brændbar (F) Ætsende (C) | ||
| NFPA 704 | |||
| R-sætninger | R11 R14 R34 | ||
| S-sætninger | S1/2 S9 S16 S26 S45 | ||
| Flammepunkt | 4 °C (277 K) | ||
| Selvantændelses-temperatur | 390 °C (663 K) | ||
| Explosionsgrænser | 7,3–19 % | ||
| Beslægtede stoffer | |||
| Andre acylklorider | Propionylklorid Butyrylklorid | ||
| Relaterede forbindelser | Eddikesyre Eddikesyreanhydrid Acetylbromid | ||
| Hvis ikke andet er angivet, er data givet for stoffer i standardtilstanden (ved 25 °C, 100 kPa) | |||
Syntese
redigérAcetylklorid blev første gang syntetiseret i 1852 af den franske kemiker Charles Frédéric Gerhardt ved reaktion mellem kaliumacetat (CH3COO−+K+) og fosforylklorid (POCl3).[1]
Ved reaktion mellem eddikesyreanhydrid og hydrogenklorid dannes en blanding af acetylklorid og eddikesyre:[2]
- (CH3CO)2O + HCl → CH3COCl + CH3CO2H
Laboratoriesyntese
redigérI laboratoriet syntetiseres acetylklorid ved reaktion mellem eddikesyre og vandsugende kloreringsreagenser som fosfortriklorid (PCl3), fosforpentaklorid (PCl5), sulfurylklorid (SO2Cl2) eller thionylklorid (SOCl2). Produktet af disse reaktioner er dog typisk forurenet med fosfor- eller svovlholdige urenheder, som kan besværliggøre efterfølgende reaktioner.[3] En alternativ syntese, der ikke danner fosfor- og svovlholdige urenheder, består i at reagere fosgen med eddikesyre:
- COCl2 + CH3COOH → CH3COCl + HCl + CO2
HCl-urenheder kan fjernes ved efterfølgende destillation af råproduktet fra dimethylanilin eller ved at gennemboble blandingen med en strøm af argon.
Andre metoder
redigérEn blanding af dikloreddikesyre (CHCl2COOH) og eddikesyre danner acetylklorid ved opvarmning.[3] Acetylklorid kan tillige dannes ved katalytisk carbonylering af metylklorid (CH3Cl).[4]
Forekomst
redigérAcetylklorid forventes ikke at forekomme i naturen, idet kontakt med vand vil hydrolysere acetylklorid til eddikesyre og hydrogenklorid. Selv i atmosfærisk luft frigiver acetylklorid hvide "dampe" som følge af hydrolyse forårsaget af fugt i luften. Disse dampe er i virkeligheden små dråber af saltsyre (HCl i vandig opløsning) og eddikesyre dannet ved hydrolyse.
Anvendelser
redigérI organisk syntese anvendes acetylklorid til acyleringsreaktioner, dvs. indførelsen af en acetylgruppe. Acetyl er en acylgruppe med formlen -C(=O)-CH3. To vigtige typer acyleringsreaktioner er esterificering og Friedel-Crafts-acylering.
Eddikesyreestre og -amider
redigérAcetylklorid anvendes som reagens i syntesen af estre og amider af eddikesyre. Ved reaktion mellem f.eks. acetylklorid og ætanol dannes esteren ethylacetat:
- CH3COCl + HO-CH2-CH3 → CH3-COO-CH2-CH3 + H-Cl
Acyleringsreaktioner af denne type udføres ofte i tilstedeværelse af en base som pyridin, triethylamin eller 4-dimethylaminopyridin, der dels fungerer som katalysator, dels neutraliserer det dannede HCl. Disse reaktioner foregå ofte via dannelsen af en midlertidig keten.
Friedel-Crafts-acyleringer
redigérEn anden vigtig type acyleringsreaktion er Friedel-Crafts-acyleringen,[5] der er et eksempel på en elektrofil aromatisk substitution.
Referencer
redigér- ^ Se:
- Gerhardt, Charles (1852) "Ueber wasserfreie organische Säuren" (Om vandfri organiske syrer), Annalen der Chemie und Pharmacie, 83 : 112–116. (tysk)
- Gerhardt, Charles (1853) "Untersuchungen über die wasserfreien organischen Säuren" (Undersøgelser af vandfri organiske syrer), Annalen der Chemie und Pharmacie, 87 : 57–84 ; se især pp. 68–71. (tysk)
- ^ Hosea Cheung, Robin S. Tanke, G. Paul Torrence. “Acetic Acid”, artikel i Ullmann's Encyclopedia of Industrial Chemistry, 2002, Wiley-VCH, Weinheim. . (engelsk)
- ^ a b Leo A. Paquette (2005). "Acetyl chloride". Handbook of Reagents for Organic Synthesis, Activating Agents and Protective Groups (engelsk). John Wiley & Sons. s. 16. ISBN 978-0-471-97927-2.
- ^ US patent 4352761 (besøgt 20. august 2016). (engelsk)
- ^ Charles Merritt, Jr and Charles E. Braun "9-Acetylanthracene" Org. Synth. 1950, 30, 2. (engelsk)
Eksterne henvisninger
redigér- International Chemical Safety Card 0210 (engelsk)